Bigger and Better Photons: The Road to Great FLIM?Results
原文鏈接 by Wolfgang Becker
翻譯 by 譚瓅
摘要:這篇文章試圖幫助bh FLIM技術(shù)的現(xiàn)有和未來用戶從FLIM實驗中獲得最佳結(jié)果。第一部分解釋了TCSPC FLIM的原理,并給出了記錄的光子分布的效果。它表明,測量壽命的信噪比在優(yōu)先取決于記錄的光子數(shù)量。第二部分重點介紹優(yōu)化光子數(shù),而不增加施加到樣品中的光應(yīng)力。我們討論了激發(fā)功率、采集時間、采集效率、數(shù)值孔徑、聚焦精度、對準(zhǔn)精度和探測器效率的影響。第三部分將重點介紹光子效率。它考慮了TCSPC計時參數(shù)、計數(shù)背景、像素數(shù)、儀器響應(yīng)函數(shù)的影響,以及多指數(shù)衰減函數(shù)的挑戰(zhàn)。最后一部分專門介紹數(shù)據(jù)分析。本文中的所有結(jié)論均通過在實際條件下記錄的真實測量數(shù)據(jù)進行演示。
第二部分:優(yōu)化(增加)光子數(shù)
激發(fā)功率
當(dāng)FLIM用戶希望增加光子數(shù)時,第一個想法通常是增加激發(fā)功率。這當(dāng)然是獲得更多光子的有效方法,但它并不總是有助于獲得更好的FLIM結(jié)果。FLIM實驗通常在熒光團濃度低的樣品上進行,原因是只有當(dāng)熒光團本身對細(xì)胞的活力或其代謝功能沒有明顯影響時,才能看到分子效應(yīng)。此外,熒光團可能具有較低的量子效率。如果增加激發(fā)功率,分子必須執(zhí)行更多的激發(fā)–發(fā)射循環(huán),結(jié)果是光漂白,形成自由基,激光誘導(dǎo)壽命變化,光損傷,甚至樣品完全被破壞。然后,成像過程不再是非侵入性的,FLIM結(jié)果變得毫無意義。因此,增加激光功率的選擇是有限的(參考文獻(xiàn)[8])。侵入性效應(yīng)的幾個例子如圖8所示。

圖8:左:Convallaria圖像,用405nm激光掃描的中心區(qū)域。中:活細(xì)胞的雙光子NADH圖像。在明亮的紅色斑點中,發(fā)生了光損傷,通過非常快速衰減的斑點表現(xiàn)出來。右圖:酵母細(xì)胞的時域馬賽克拼接FLIM圖像,采用780nm雙光子激發(fā)。記錄從左下角開始,一直到拼接圖的右上角。破壞從第8和9格開始,一直持續(xù)到第16格。
采集時間
與增加激發(fā)功率不同,增加采集時間通常是一種不錯的選擇,損傷效果是高度非線性的。通常,可以用僅略低于損傷閾值的功率長時間掃描樣品,可增加光子數(shù),所需要的只是實驗者的耐心。圖 9 顯示了一個示例。左邊的圖像采集時間為1分鐘,右邊的圖像采集時間為2分鐘。結(jié)果是,右邊的圖像包含2倍以上的光子。正如預(yù)期的那樣,它還提供了1.4倍的壽命SNR,參考圖像下方的壽命直方圖。

圖9:以不同的采集時間對同一樣品進行成像,左圖 1 分鐘,右圖2 分鐘。圖像格式512×512像素,1024個時間通道。
雖然光子數(shù)(以及壽命精度)和采集時間的相關(guān)性是微不足道的,但FLIM用戶通常不會意識到這一點。特別是來自傳統(tǒng)基于強度的成像的用戶,當(dāng)達(dá)到強度圖像的合理SNR時,往往會停止采集。但是,這存在一個謬誤。當(dāng)強度圖像每像素包含不超過幾十個光子時,它開始看起來不錯。這種圖像的SNR可能足以區(qū)分不同的熒光團,但不足以從熒光壽命中得出所需的分子信息。因此,請確保采集時間足夠長。我們的SPCM采集軟件提供了許多選項,用于在采集過程中查看光子數(shù)。您可以在所選像素或感興趣區(qū)域中顯示衰減曲線,可以在最亮的像素和所選像素中顯示光子數(shù),并且可以在線顯示壽命圖像。請參見圖 10,使用這些選項,您應(yīng)該能確定到目前為止記錄的數(shù)據(jù)是否足以進行進一步分析。如有不夠,請記錄更長時間。

圖10:SPCM幫助用戶確定是否記錄了足夠光子數(shù)的功能。從左到右:在線壽命圖像,選定位置的衰減曲線,最亮像素(頂部)中的光子數(shù)和數(shù)據(jù)點位置的光子數(shù)。
有時有人反對說,當(dāng)要觀察生理變化時,無法采用較長的采集時間。然而,如果使用適當(dāng)?shù)亩嗑STCSPC技術(shù),這并不一定,請看(參考文獻(xiàn)[2,9])。
顯微物鏡
顯微鏡物鏡的數(shù)值孔徑對探測效率有顯著影響。熒光以各向同性方式發(fā)射,只有一部分被顯微物鏡收集。從理論上講,收集效率隨著數(shù)值孔徑的增加而成平方倍增加。這意味著NA 1.25的物鏡應(yīng)該比NA 0.5的物鏡收集6倍以上的光子數(shù)。但在實踐中,差異會小一些,因為高數(shù)值孔徑物鏡具有更多的光學(xué)元件和更低的透過率。然而,收集效率的差異是驚人的。圖 11 顯示了一個示例。兩幅圖像都采用單光子激發(fā)和共聚焦探測記錄的。左圖像用NA 0.5的x20空氣鏡記錄,右圖像用NA 1.25的x63油鏡記錄。使用高數(shù)值孔徑物鏡記錄的圖像包含的光子是低數(shù)值孔徑下記錄的圖像的三倍。
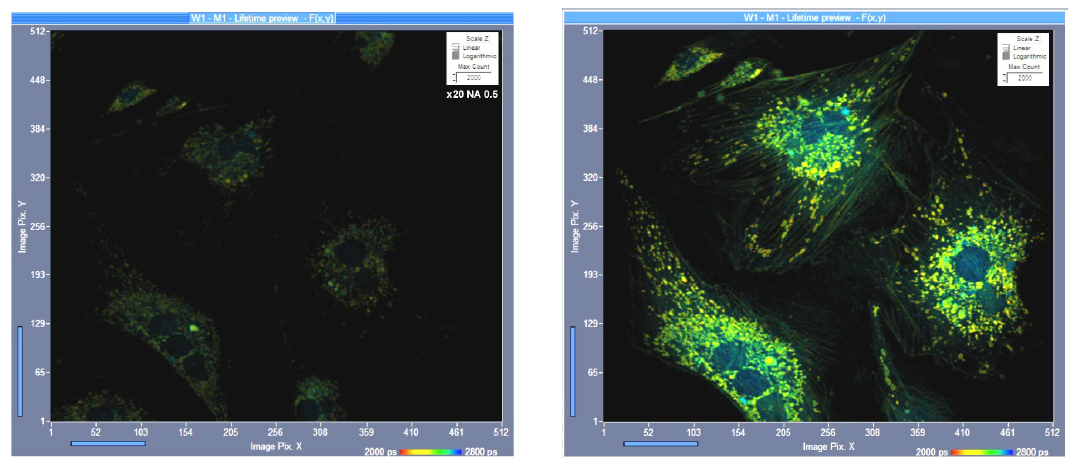
圖11:使用不同NA的物鏡記錄的FLIM圖像,相同的強度尺度,單光子激發(fā),共聚焦探測。左:X20 空氣鏡,NA 0.5,右:X63油鏡,NA 1.25.
聚焦
對焦不佳通常被認(rèn)為是空間分辨率欠佳的來源,同時,它對探測效率也有顯著影響。圖 12 顯示了一個示例,兩幅圖像均通過共聚焦掃描記錄,針孔尺寸相同,采集時間相同。左圖略微失焦,盡管如此,圖像清晰度只是略受損。右圖完全對焦。可以很容易地看出,正確對焦的圖像更亮。與失焦圖像相比,光子的數(shù)量大約高出1.5倍。由于FLIM系統(tǒng)顯示強度歸一化圖像(這樣做是因為強度的差異可能時數(shù)量級的),因此通常不會注意到這些差異。因此,當(dāng)您在“預(yù)覽”模式下進行最終對焦時,請花幾秒鐘在關(guān)閉自動縮放功能的情況下優(yōu)化對焦。

圖 12:左圖略微失焦,右圖完全對焦。相同強度尺度,單光子激發(fā),共聚焦探測。雖然失焦圖像中的圖像清晰度僅略受損,但光子數(shù)僅為完美圖像中光子數(shù)的60%。圖像格式512 x 512像素,1024個時間通道。
光學(xué)系統(tǒng)的對準(zhǔn)
光學(xué)系統(tǒng)的對準(zhǔn)對探測效率有巨大的影響,共聚焦系統(tǒng)尤其如此。共聚焦對準(zhǔn)非常關(guān)鍵,幾乎沒有一個共聚焦系統(tǒng)可以長時間保持完美對準(zhǔn)。圖 13 顯示了一個示例,左邊的圖像是在針孔對準(zhǔn)稍微偏離的情況下采集的,幾乎在任何共聚焦系統(tǒng)中都可以發(fā)現(xiàn)這樣水平的失準(zhǔn)。通常,它不被注意到,因為圖像清晰度幾乎沒有受到損害。然而,與來自完美對準(zhǔn)系統(tǒng)的圖像進行比較(圖13,右),記錄的光子數(shù)量存在明顯的損失。某些情況的失準(zhǔn)甚至導(dǎo)致圖像清晰度可見的下降,可導(dǎo)致光子數(shù)的巨大損失,在這些情況下,效率下降一個數(shù)量級甚至更多并不罕見。
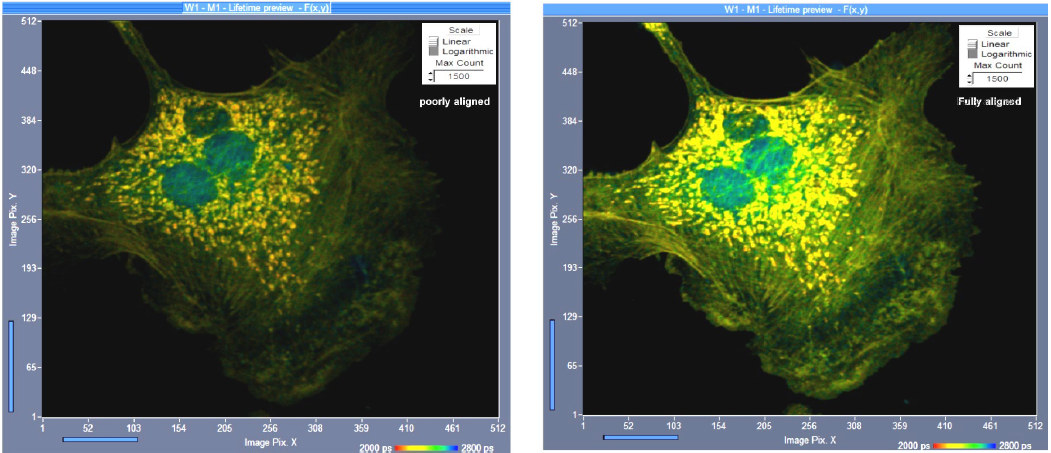
圖 13:共聚焦對準(zhǔn)的效果。左:略微失準(zhǔn)。右:完美對準(zhǔn)。雖然不對準(zhǔn)尚未導(dǎo)致圖像清晰度的可見下降,但它會導(dǎo)致50%的光子損失。
在非解掃探測(NDD)的多光子系統(tǒng)中,失準(zhǔn)甚至也可能導(dǎo)致影響。雖然這些系統(tǒng)的探測光路很可靠,很少失準(zhǔn),但激發(fā)光路卻存在失準(zhǔn)的可能。多光子顯微鏡的飛秒激光需要空間光耦合到掃描頭中,這為光路提供了許多可能偏離對準(zhǔn)的可能,這導(dǎo)致激光不再集中在顯微物鏡的后孔徑中間。結(jié)果,聚焦質(zhì)量下降,激發(fā)效率降低,光漂白和光損傷并不總是以相同的比例減少,特別是如果樣品在激光的本身的波長上有一定的吸收。因此,多光子系統(tǒng)也應(yīng)該定期重新對準(zhǔn)。這可以通過檢查激光束在物鏡后孔徑上的位置,并將其調(diào)回中心來輕松完成。
探測器
多年來,激光掃描顯微鏡,特別是FLIM系統(tǒng),一直使用傳統(tǒng)的光電倍增管(PMT)作為探測器。PMT具有較大的有效面積,每平方毫米有效面積的暗計數(shù)率極低,并且有足夠的增益和速度來探測單個光子。具有常規(guī)光陰極的PMT的光陰極的量子效率約為20%,然而,并非每個由陰極發(fā)射的光電子都進入放大系統(tǒng)并提供有用的單電子脈沖。因此,凈效率約為15%。隨著采用帶有GaAsP陰極的PMT,效率有所提高,這些陰極的量子效率接近50%。如濱松的H7422 GaAsP PMT,已經(jīng)用于FLIM多年。然而,這些探測器的儀器響應(yīng)(IRF)寬度約為250至350 ps,這對于高端FLIM應(yīng)用來說是不夠的。隨著濱松R10467-40混合型PMT的推出,情況完全改變了,混合型PMT的原理保證了幾乎所有離開陰極的光電子都能提供單電子脈沖。憑借其GaAsP光電陰極,R10467-40的凈探測效率達(dá)到50%。IRF快速而干凈,并且沒有像傳統(tǒng)PMT那樣的后脈沖背景。但R10467-40不易使用,它需要 -8000 V 和 +400 V 電源電壓、可靠的過載保護、高增益前置放大器和出色的射頻屏蔽。bh是第一個解決這些問題的公司,并將這種探測器完全應(yīng)用到其FLIM系統(tǒng)(參考文獻(xiàn)[11])。不同探測器效率的比較可以在“bh TCSPC手冊”(參考文獻(xiàn)[2])的“TCSPC探測器”一章中找到。
圖 14 顯示了一個實際示例。左邊的圖像是用傳統(tǒng)的PMT(bh PMC-100-0模塊)記錄的,右邊的圖像是用GaAsP混合型PMT(bh HPM-100-40模塊)記錄的。采用GaAsP混合探測器的光子數(shù)約為4.2倍。

圖 14:使用傳統(tǒng) PMT(bh PMC-100-0,左)和混合型 PMT(bh HPM-100-40,右)記錄的 FLIM 圖像。相同的成像條件,相同的采集時間。HPM-100-40圖像包含的光子是使用傳統(tǒng)PMT拍攝的圖像的4.2倍。
像素數(shù)
獲得的壽命的SNR與每個像素的光子數(shù)成正比。因此,原則上,光子限制條件下的SNR可以通過減少像素數(shù)量來增加。例如,128 x 128 像素的圖像只需要 512 x 512 像素圖像的 1/16 光子。這種方法的缺陷在于,它用壽命精度與空間分辨率進行了權(quán)衡。除非有其他使用低像素數(shù)的必要(例如限制的數(shù)據(jù)大小或需要快速掃描),否則不建議將像素數(shù)降低到256 x 256 以下。更好的方法是使用足夠空間采樣的像素數(shù)記錄圖像,而在數(shù)據(jù)分析中使用像素合并(參考文獻(xiàn)[3]),有關(guān)詳細(xì)信息,請參閱第四部分——“數(shù)據(jù)分析”。數(shù)據(jù)分析中的像素合并使像素數(shù)保持不變,但會對當(dāng)前像素及其周圍像素的衰減數(shù)據(jù)之和運行壽命分析。
其優(yōu)點是空間分辨率沒有損失,也沒有空間欠采樣,并且您可以自由地在記錄的數(shù)據(jù)上選擇最佳的像素合并因子。圖 15 顯示了一個示例。頂行的數(shù)據(jù)以128 x 128像素掃描記錄,底行的數(shù)據(jù)通過512 x 512像素掃描記錄,兩個記錄都包含相同的光子總數(shù)。因此,512 x 512 像素掃描的每像素光子數(shù)要低 16 倍。然而,較低的光子數(shù)可通過數(shù)據(jù)分析軟件中的像素合并來補償?shù)摹R虼耍總€合并區(qū)域(底行)的衰減曲線包含與每個像素衰減曲線(頂行)相同的光子數(shù)。因此,兩個記錄的壽命直方圖(如右圖所示)具有相同的寬度。但是,來自512 x 512像素掃描的圖像(底行,左)比來自128 x 128像素掃描的圖像(頂行,左)清晰得多。請參閱“數(shù)據(jù)分析”部分。

圖 15:使用不同像素數(shù)記錄的 FLIM 數(shù)據(jù)。相同的采集時間,相同的光子總數(shù),上行128 x 128 像素,下行 512 x 512 像素。從左到右:圖像、光標(biāo)位置的衰減曲線、壽命直方圖。使用像素合并對512 x 512像素的圖像進行分析,以補償每像素的較低光子數(shù)。
References
1. W. Becker, Advanced time-correlated single-photon counting techniques. Springer, Berlin, Heidelberg, New York,2005
2. W. Becker, The bh TCSPC handbook, 8th edition. Becker & Hickl GmbH (2019), available online on www.becker-hickl.com. Please contact bh for printed copies.
3. SPCImage NG data analysis software. In: W. Becker, The bh TCSPC handbook, 8th edition. Becker & Hickl GmbH(2019)
4. W. Becker (ed.), Advanced time-correlated single photon counting applications. Springer, Berlin, Heidelberg, New York (2015)
5. Becker & Hickl GmbH, DCS-120 Confocal and Multiphoton Scanning FLIM Systems, user handbook 87th ed. (2019).?Available on www.becker-hickl.com
6. Becker & Hickl GmbH, Modular FLIM systems for Zeiss LSM 510 and LSM 710 family laser scanning microscopes.?User handbook. Available on www.becker-hickl.com
7. Becker & Hickl GmbH, FLIM systems from Zeiss LSM 980 Laser scanning microscopes, addendum to modular FLIM?systems for Zeiss LSM 510 and LSM 710 family laser scanning microscopes. Available on www.becker-hickl.com
8. Fast-Acquisition TCSPC FLIM: What are the Options? Application note, available from www.becker-hickl.com
9. W. Becker, V. Shcheslavkiy, S. Frere, I. Slutsky, Spatially Resolved Recording of Transient Fluorescence-Lifetime?Effects by Line-Scanning TCSPC. Microsc. Res. Techn. 77, 216-224 (2014)
10. R.M. Ballew, J.N. Demas, An error analysis of the rapid lifetime determination method for the evaluation of single?exponential decays, Anal. Chem. 61, 30 (1989)
11. W. Becker, B. Su, K. Weisshart, O. Holub, FLIM and FCS Detection in Laser-Scanning Microscopes: Increased?Efficiency by GaAsP Hybrid Detectors. Micr. Res. Tech. 74, 804-811 (2011)
12. Wolfgang Becker, Cornelia Junghans, Axel Bergmann, Two-photon FLIM of mushroom spores reveals ultra-fast decay component. Application note, available on www.becker-hickl.com.
13. Becker & Hickl GmbH, Ultra-fast HPM detectors improve NADH FLIM. Application note, www.becker-hickl.com
14. Becker & Hickl GmbH, Two-Photon FLIM with a Femtosecond Fibre Laser. Application note, www.becker-hickl.com
15. Becker Wolfgang, Suarez-Ibarrola Rodrigo, Miernik Arkadiusz, Braun Lukas, Metabolic Imaging by Simultaneous?FLIM of NAD(P)H and FAD. Current Directions in Biomedical Engineering 5(1), 1-3 (2019)
16. H.C. Gerritsen, M.A.H. Asselbergs, A.V. Agronskaia, W.G.J.H.M. van Sark, Fluorescence lifetime imaging in?scanning microscopes: acquisition speed, photon economy and lifetime resolution, J. Microsc. 206, 218-224 (2002)
17. M. K?llner, J. Wolfrum, How many photons are necessary for fluorescence-lifetime measurements?, Phys. Chem. Lett.?200, 199-204 (1992)
18. I. Isenberg, R.D. Dyson, The analysis of fluorescence decay by a method of moments. Biophys. J. 9, 1337-1350 (1969)
